| 序號 |
區(qū)域 |
年份 |
通用名 |
類型 |
規(guī)格 |
劑型 |
生產(chǎn)廠家 |
轉(zhuǎn)化系數(shù) |
批準(zhǔn)文號 |
價格 |
來源項目 |
操作 |
| 561 |
甘肅 |
2025 |
乳酸環(huán)丙沙星氯化鈉注射液 |
最終中標(biāo) |
100ml:乳酸環(huán)丙沙星0.2g(按C17H18FN3O3計)與氯化鈉0.9g |
注射劑 |
四川太平洋藥業(yè)有限責(zé)任公司 |
1 |
國藥準(zhǔn)字H20066255 |
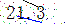
|
2025年甘肅省關(guān)于2025年第四批國家和聯(lián)盟集采相關(guān)藥品企業(yè)申報結(jié)果公布表
|
詳情 |
| 562 |
甘肅 |
2025 |
注射用氨芐西林鈉 |
最終中標(biāo) |
按C16H19N3O4S計算0.5g |
注射劑 |
哈藥集團制藥總廠 |
1 |
國藥準(zhǔn)字H23020926 |
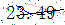
|
2025年甘肅省關(guān)于2025年第四批國家和聯(lián)盟集采相關(guān)藥品企業(yè)申報結(jié)果公布表
|
詳情 |
| 563 |
甘肅 |
2025 |
注射用氨芐西林鈉舒巴坦鈉 |
最終中標(biāo) |
0.75g(C??H??N?O?S0.5g與C?H??NO?S0.25g) |
注射劑 |
海南通用三洋藥業(yè)有限公司 |
1 |
國藥準(zhǔn)字H10970144 |
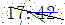
|
2025年甘肅省關(guān)于2025年第四批國家和聯(lián)盟集采相關(guān)藥品企業(yè)申報結(jié)果公布表
|
詳情 |
| 564 |
甘肅 |
2025 |
乳酸環(huán)丙沙星氯化鈉注射液 |
最終中標(biāo) |
按環(huán)丙沙星計100mL:環(huán)丙沙星0.2g與氯化鈉0.9g |
注射液 |
Bayer AG |
1 |
國藥準(zhǔn)字J20130176 |
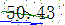
|
2025年甘肅省關(guān)于2025年第四批國家和聯(lián)盟集采相關(guān)藥品企業(yè)申報結(jié)果公布表
|
詳情 |
| 565 |
甘肅 |
2025 |
尼莫地平注射液 |
最終中標(biāo) |
50ml:10mg |
注射劑 |
Solupharm Pharmazeutische Erzeugnisse GmbH |
1 |
國藥準(zhǔn)字J20140105 |
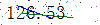
|
2025年甘肅省關(guān)于2025年第四批國家和聯(lián)盟集采相關(guān)藥品企業(yè)申報結(jié)果公布表
|
詳情 |
| 566 |
甘肅 |
2025 |
瑞戈非尼片 |
最終中標(biāo) |
40mg |
片劑 |
Bayer AG |
28 |
國藥準(zhǔn)字HJ20171300 |
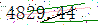
|
2025年甘肅省關(guān)于2025年第四批國家和聯(lián)盟集采相關(guān)藥品企業(yè)申報結(jié)果公布表
|
詳情 |
| 567 |
甘肅 |
2025 |
注射用鹽酸羅沙替丁醋酸酯 |
最終中標(biāo) |
75mg |
注射劑 |
江蘇金絲利藥業(yè)股份有限公司 |
1 |
國藥準(zhǔn)字H20234148 |
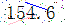
|
2025年甘肅省關(guān)于2025年第四批國家和聯(lián)盟集采相關(guān)藥品企業(yè)申報結(jié)果公布表
|
詳情 |
| 568 |
甘肅 |
2025 |
阿司匹林腸溶片 |
最終中標(biāo) |
100mg |
腸溶片 |
Bayer HealthCare Manufacturing S.r.l. |
30 |
國藥準(zhǔn)字HJ20160685 |
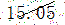
|
2025年甘肅省關(guān)于2025年第四批國家和聯(lián)盟集采相關(guān)藥品企業(yè)申報結(jié)果公布表
|
詳情 |
| 569 |
甘肅 |
2025 |
哌柏西利膠囊 |
最終中標(biāo) |
125mg |
膠囊劑 |
江蘇豪森藥業(yè)集團有限公司 |
21 |
國藥準(zhǔn)字H20223445 |
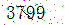
|
2025年甘肅省關(guān)于2025年第四批國家和聯(lián)盟集采相關(guān)藥品企業(yè)申報結(jié)果公布表
|
詳情 |
| 570 |
甘肅 |
2025 |
氫溴酸伏硫西汀片 |
最終中標(biāo) |
10mg(按C??H??N?S計) |
薄膜衣片 |
江蘇豪森藥業(yè)集團有限公司 |
14 |
國藥準(zhǔn)字H20223303 |
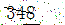
|
2025年甘肅省關(guān)于2025年第四批國家和聯(lián)盟集采相關(guān)藥品企業(yè)申報結(jié)果公布表
|
詳情 |